Thalidomid: der Wirkstoff von Contergan
und seine Folgen
Der Wirkstoff von Contergan heißt Thalidomid. Die Substanz wurde 1954 in unseren Laboren entwickelt. Wurde die Substanz während einer bestimmten Phase im ersten Drittel der Schwangerschaft eingenommen, konnte sie zu Missbildungen bei ungeborenen Kindern führen, die später als "Contergan-Babys" bekannt wurden.
Auf dieser Seite bieten wir einen Überblick über den Wirkstoff. Wir erläutern, was genau Thalidomid ist, wie es entwickelt wurde und wie es im Körper wirkt. Außerdem gehen wir auf die Frage ein, warum nicht bereits vor der Markteinführung entdeckt wurde, dass das Medikament Fehlbildungen bewirken kann. Abschließend geben wir einen kurzen Überblick darüber, wie Thalidomid heute eingesetzt wird.
Inhalt
Die chemische Zusammensetzung von Thalidomid
Welche Nebenwirkungen hat Thalidomid?
Thalidomid kann Fehlbildungen bei ungeborenen Kindern verursachen
Wie die moderne Wissenschaft die Wirkung von Thalidomid erklärt
Die artspezifische Wirkung von Thalidomid
Polyneuritis: Thalidomid kann die Nerven schädigen
Wurde Thalidomid im Nationalsozialismus entwickelt?
Die chemische Zusammensetzung von Thalidomid
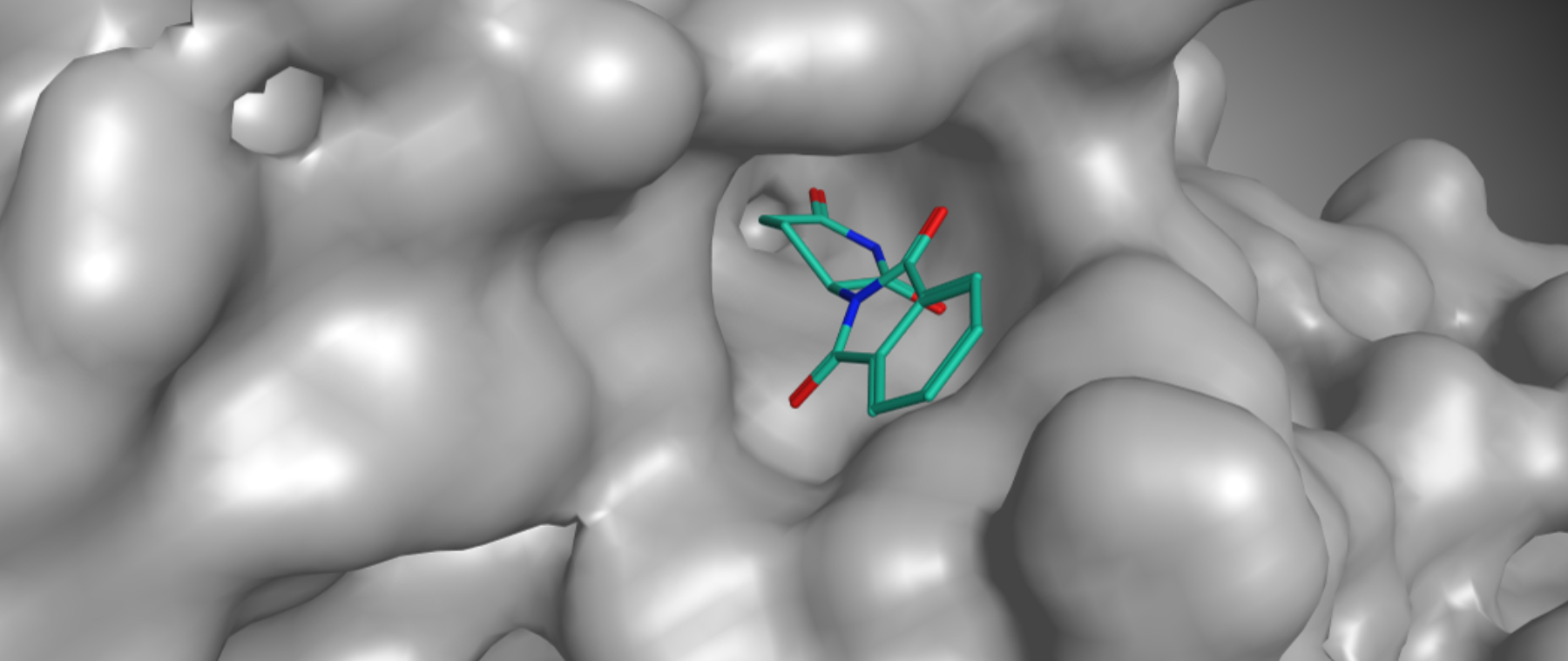
Thalidomid ist ein Derivat der Glutaminsäure. Es ist ein leicht wasserlöslicher, kristalliner Feststoff mit der Strukturformel C13H10N2O4.
Die chemische Verbindung Thalidomid ist chiral. Das bedeutet, dass sie in zwei Formen, den sogenannten Enantiomeren, vorliegen kann. Wie man später herausgefunden hat, ist nur eines dieser Enantiomere fruchtschädigend (teratogen) und ruft Fehlbildungen beim Embryo hervor.
Spätere Forschungen haben allerdings gezeigt, dass sich die beiden Formen (Enantiomere) im Körper innerhalb weniger Stunden ineinander umwandeln. Selbst wenn man nur die nicht-teratogene Form verabreicht, liegen im Körper innerhalb weniger Stunden wieder beide Formen vor. Mit anderen Worten: Durch die Gabe der zunächst nicht-teratogenen Form lässt sich die teratogene Wirkung von Thalidomid im Körper nicht verhindern.
Wie wirkt Thalidomid?
Der Wirkstoff Thalidomid hat viele Eigenschaften. Einige davon sind durchaus positiv: Es wirkt beruhigend und schlafauslösend, zudem hat es antientzündliche Eigenschaften und hemmt das Wachstum mancher Krebszellen.
Bei der Erfindung Thalidomids im Jahr 1954 fanden unsere damaligen Forscher heraus, dass die Einnahme von Thalidomid müde macht und beruhigt. Sie entdeckten auch, dass es nicht möglich war, eine letale – also tödliche – Dosis des Stoffs zu verabreichen. Da alle anderen damals gängigen Schlafmittel bei einer Überdosierung zum Tode führen konnten, galt Thalidomid als eine bedeutende Entdeckung.
Wie löst Thalidomid seine beruhigende Wirkung aus? Vereinfacht ausgedrückt scheint Thalidomid einen körpereigenen Botenstoff nachzuahmen, welcher die Informationsübertragung zwischen den Nervenzellen im Körper hemmt. Dadurch kommen weniger Signale im Gehirn an, was einen entspannenden und einschläfernden Effekt auf den Körper hat.1
Aufgrund dieser Wirkung wurde Thalidomid als Wirkstoff des Medikaments Contergan eingesetzt. Nach unseren Erkenntnissen entsprachen die Entwicklung und Einführung von Contergan dem damals gültigen Wissen und den geltenden Standards der pharmazeutischen Industrie.
Welche Nebenwirkungen hat Thalidomid?
Nachdem Thalidomid auf den Markt gebracht wurde, stellte sich heraus, dass der Stoff schwere Nebenwirkungen hervorrufen kann, darunter die als „Contergan-Schäden“ bekannten Fehlbildungen. Im Folgenden gehen wir genauer auf die Nebenwirkungen von Thalidomid ein.Thalidomid kann Fehlbildungen bei ungeborenen Kindern verursachen
Wird Thalidomid in der Schwangerschaft zwischen dem 34. und dem 50. Tag nach dem ersten Tag der letzten Regelblutung eingenommen, führt es zu den als Thalidomid-Schäden bekannten Fehlbildungen.
Zu den Thalidomid-Schäden gehören unter anderem:
- Verkürzung oder völliges Fehlen von Armen und Beinen
- Fehlbildungen an Händen und Füßen
- Fehlbildungen an Hüfte, Verdauungstrakt und Genitalien
- Fehlbildungen oder völliges Fehlen der Ohrmuscheln
Wie die moderne Wissenschaft die Wirkung von Thalidomid erklärt
Der Wirkmechanismus von Thalidomid – und damit die Erklärung, warum die Fehlbildungen überhaupt auftreten – blieb jahrzehntelang unbekannt. Die Grundlage für die Aufklärung der Wirkung haben die Arbeitsgruppen von Takumi Ito und Hideki Ando vom Tokyo Institute of Technology sowie Yamaguchi von der Tokyo Medical University u. a. im Jahr 2010 gelegt. 2 Diese Erkenntnisse sind von verschiedenen internationalen Forscherteams ergänzt worden. Bis heute ergeben sich laufend neue Erkenntnisse. 3
Nach dem aktuellen Wissensstand ruft Thalidomid die als „Contergan-Schäden“ bekannten Fehlbildungen hervor, weil es als Bindeglied bestimmte Proteine zusammenführt, die im Körper des Kindes unter anderem die Ausbildung der Extremitäten steuern. Diese Verbindung hat zur Folge, dass sich der Körper des Kindes nicht mehr vollständig entwickeln kann.
Jede Zelle des menschlichen Körpers enthält Proteine.4 Sie dienen als molekulare „Werkzeuge“ und können verschiedene Aktionen ausführen, wie zum Beispiel Gene an- oder ausschalten, Zellbewegungen ermöglichen oder Signalstoffe erkennen.
Bei der Wirkweise von Thalidomid spielen drei Arten von Proteinen eine Rolle5:
- Das Protein Cereblon kann andere Proteine anziehen, quasi wie ein Magnet6. Diese Proteine werden anschließend von Cereblon „markiert“ und abgebaut, das heißt vernichtet.7
- Die Proteine Sall 4 und p63 sind sogenannte Transkriptionsfaktoren. Wie ein Schalter können sie Gene ein- und ausschalten. Im Körper des Kindes steuern Sall 4 und p63 das Wachstum und die Entwicklung der Extremitäten und bestimmter Organe.
Die Strukturen von Cereblon und Sall 4 bzw. p63 sind so verschieden, dass sie im Originalzustand nicht zueinander passen. Sie existieren nebeneinander. In diesem Zustand können Sall 4 und p63 das Wachstum der Extremitäten anregen und die Ausbildung von Organen steuern.
Wird Thalidomid während eines bestimmten Zeitrahmens während der Schwangerschaft eingenommen, kann der Wirkstoff über den Stoffwechsel der Mutter in den Körper des Kindes gelangen. Dort angekommen, dockt Thalidomid zunächst an das Cereblon an. An dieser Stelle entsteht eine teilweise andere, neuartige Struktur, an die Sall 4 und p63 andocken können.
Das Video des Dana-Farber Cancer Instituts erklärt die Vorgänge. Der im Film formulierte Hinweis, dass das Medikament gegen Schwangerschaftsübelkeit entwickelt worden sei, ist jedoch unzutreffend.
Die artspezifische Wirkung von Thalidomid
Nachdem Contergan vom Markt genommen worden war, versuchten Forscher zunächst, den Verdacht der fruchtschädigenden Wirkung an den damals für Arzneimitteltests üblicherweise verwendeten Labortieren nachzuweisen, nämlich an Ratten, Kaninchen und Mäusen. Die Ergebnisse fielen zunächst negativ aus. Grund dafür ist die artspezifische Wirkung von Thalidomid: Thalidomid bewirkt nicht bei allen Tieren, sondern nur bei bestimmten Arten Fehlbildungen. Fruchtschäden bei schwangeren Tieren konnten deshalb erst 1962 beobachtet werden, nach der Marktentnahme von Contergan, als man Thalidomid gezielt an einer besonderen Kaninchenrasse testete, dem Weißen Neuseeländer.
Polyneuritis: Thalidomid kann die Nerven schädigen
Thalidomid kann bei den Anwendern des Arzneimittels Polyneuritis hervorrufen, eine entzündliche Erkrankung des Nervensystems. Zu den Symptomen gehören ein Taubheitsgefühl in den Finger- und Fußspitzen; zudem kann eine Polyneuritis auch sehr schmerzhaft sein. Bei länger andauernden Beschwerden führt Polyneuritis zu einer pathologisch nachweisbaren Veränderung des Nervengewebes.
Wurde Thalidomid im Nationalsozialismus entwickelt?
Grünenthal verurteilt die Gräueltaten des Nazi-Regimes auf das Schärfste und hat sich in der Vergangenheit immer wieder in Initiativen gegen Rechtsradikalismus engagiert. Wie in vielen anderen Firmen haben jedoch auch bei Grünenthal in der Nachkriegszeit Personen gearbeitet, die zuvor auch Positionen in der NSDAP innehatten.
Einige Verschwörungstheoretiker leiten unter anderem davon ab, dass Thalidomid bereits während der Zeit des Nationalsozialismus von NS-Chemikern entwickelt und an KZ-Häftlingen als Gegenmittel für chemische Kampfstoffe getestet wurde. Für diese Spekulationen gibt es keine belastbaren Belege.8 Wir gehen hier auf zwei immer wieder geäußerte Theorien etwas genauer ein:
- Es hält sich das Gerücht, dass Thalidomid bereits vor 1954 in der Zeit des Nazi-Regimes entwickelt wurde. Originaldokumente (Laborbericht Keller, Laborbericht Kunz) sowie die unter Eid gemachten Zeugenaussagen der Grünenthal-Forscher Dr. Kunz und Dr. Keller im Contergan-Strafprozess9 belegen jedoch, dass die beiden Wissenschaftler den Wirkstoff Thalidomid im Jahr 1954 im Grünenthal-Labor entwickelten. Das erste Patent wurde 1954 eingereicht.
- Ebenso wird immer wieder versucht, eine Verbindung zwischen der Entwicklung des Wirkstoffs Thalidomid und der Nazivergangenheit des späteren Beiratsmitglieds Dr. Otto Ambros herzustellen. Dr. Ambros war jedoch nie Angestellter der Firma Grünenthal. Er trat 1972 in den Beirat von Grünenthal ein, also elf Jahre nachdem Contergan vom Markt genommen wurde.
In einem 2016 erschienenen Forschungsbericht beschäftigte sich der Historiker Dr. Niklas Lenhard-Schramm mit einer möglichen Verbindung zwischen Thalidomid und dem Nazi-Regime sowie der Glaubwürdigkeit der aufgestellten Theorien. Er kam zu dem Schluss, dass es sich bei der Theorie, Thalidomid sei bereits vor dem Jahr 1954 entwickelt worden, um verschwörungstheoretische Behauptungen ohne belastbare Beweise handle. 10
Wurde Thalidomid auch in anderen Ländern verkauft?
Nachdem Contergan in Deutschland 1957 auf den Markt gebracht wurde, vertrieben nach und nach Lizenznehmer und Distributionspartner Thalidomid-haltige Medikamente weltweit in vielen Ländern. Die Produkte kamen mit unterschiedlichen Markennamen auf den Markt, etwa Distaval und Softenon. Zudem vertrieben Unternehmen Medikamente mit dem Wirkstoff Thalidomid ohne Beteiligung oder Genehmigung von Grünenthal beispielsweise in Spanien, Italien und Brasilien.
Im November 1961 stoppte Grünenthal den Verkauf seiner Thalidomid-haltigen Produkte und informierte seine Vertriebspartner und Lizenznehmer in den jeweiligen Ländern, in denen sie die Medikamente vertrieben hatten.
Wird Thalidomid heute noch eingesetzt?
An Thalidomid wird bis heute weiter geforscht. Dabei fand man heraus, dass Thalidomid bei schweren Krankheiten wie Lepra, Knochenmarkkrebs und einigen Autoimmunkrankheiten positive Eigenschaften aufweist.11,12,13
Unser Unternehmen stellt heute keine Thalidomid-haltigen Produkte mehr her. Thalidomid ist allerdings vergleichsweise einfach zu produzieren und unterliegt keinem Patentschutz. Zu Dritten, die Thalidomid-haltige Präparate anbieten, hat Grünenthal keine Verbindung. Wissenschaft, Industrie und Regulierungsbehörden wissen heute natürlich um die schweren Nebenwirkungen, die Thalidomid auslösen kann. Herstellung und Anwendung des Wirkstoffs unterliegt daher strengen Auflagen. Das Präparat darf nur entsprechend einem speziellen Programm verschrieben und abgegeben werden, um Fehlbildungen an ungeborenem Leben zu verhindern.14
1https://www.netdoktor.de/medikamente/thalidomid/
2Takumi Ito, Hideki Ando et al (2010): “Identification of a Primary Target of Thalidomide Teratogenicity”, in: Science (327 / 5971), S.1345-1350, abrufbar unter https://science.sciencemag.org/content/327/5971/1345.
3 Tomoko Asatsuma-Okumura, Hideki AndoNature et al (2019): “p63 is a cereblon substrate involved in thalidomide teratogenicity”, in: Nature Chemical Biology (15), S. 1077–1084, abrufbar unter https://www.nature.com/articles/s41589-019-0366-7.
4 Ein Protein (umgangssprachlich Eiweiß), ist ein biologisches Makromolekül, das bis zu mehreren hundert Aminosäuren enthalten kann, die über Peptidbindungen miteinander verbunden sind. Cereblon enthält beispielsweise ca. 440 Aminosäuren.
5 Die p63-Proteine sind ∆Np63α und TAp63α. Der Abbau des Proteins ∆Np63αführt mit zu Schäden an den Gliedmaßen, während der Abbau des Proteins TAp63α mit für Defekte an den Ohren verantwortlich ist. (Nature Chemical BIOLOGY | VOL 15 | NOVEMBER 2019 | 1077–1084 https://www.nature.com/articles/s41589-019-0366-7 (study published in Nature Chemical Biology))
6 Cereblon wirkt als ein Substratrezeptor innerhalb der sogenannten E3-Ubiquitin-Ligase-Familie.
7 Cereblon gehört zu der sogenannten E3-Ubiquitin-Familie. Jede E3-Ubiquitin-Ligase kann bestimmte Proteine mit Ubiquitin markieren und so der Zelle signalisieren, dass diese markierten Proteine abgebaut/vernichtet werden sollen. Dies sind zum Beispiel fehlerhafte oder gealterte Proteine. So wird etwa die Lebensdauer von Proteinen über diesen Mechanismus gesteuert.
8 Niklas Lenhard-Schramm (2016): „Die Haltung des Landes Nordrhein-Westfalen zu Contergan und den Folgen“, Forschungsbericht der WWU Münster für das Ministerium für Gesundheit, Emanzipation, Pflege und Alter des Landes Nordrhein-Westfalen, S. 26f.
9Dagmar und Karl-Heinz Wenzel (1968): „Bericht und Protokollauszüge vom 51.-100. Verhandlungstag“, in: Der Conterganprozess (II); Keller Seite 56ff, Kunz Seite 71ff.
10Niklas Lenhard-Schramm (2016): „Die Haltung des Landes Nordrhein-Westfalen zu Contergan und den Folgen“, Forschungsbericht der WWU Münster für das Ministerium für Gesundheit, Emanzipation, Pflege und Alter des Landes Nordrhein-Westfalen, S. 26f.
11https://www.emedicinehealth.com/drug-thalidomide/article_em.htm
12David Millrine, Tadamitsu Kishimoto (2017): “A Brighter Side to Thalidomide: Its Potential Use in Immunological Disorders”, in: Trends in Molecular Medicine, (23 / 4), S. 348ff, abrufbar unter https://www.cell.com/trends/molecular-medicine/pdf/S1471-4914(17)30025-4.pdf.
13https://www.netdoktor.de/medikamente/thalidomid
14https://www.ema.europa.eu/en/medicines/human/EPAR/thalidomide-celgenehttps://www.ema.europa.eu/en/documents/overview/thalidomide-celgene-epar-medicine-overview_de.pdf
Das könnte Sie auch interessieren: